| �ϴ�����ݿ��ѧ | ��˷�����admin | ����ʱ�䣺2016-1-19 9:41:53 | ���������841�� |
����ʡ2013��2015���п���ѧ��������ࣨ�����棩������������ͼ�
��2015�꣩
һ��ѡ����
1.��2015•��ɳ������˵��������ǣ�������
�� A�� ��pH��ֽ��ô�����Һ��pHΪ9
�� B�� ��ϡ�����ȥ�����������
�� C�� ����ʯ�Ҹ�����������
�� D�� Ũ��������ˮ�ԣ������ڸ����
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��Ũ��������ʼ�Ũ�����ϡ�ͣ���Ļ�ѧ���ʣ�����������Ժ���;��
ר�⣺ �������� ���ͨ�ԣ������ļ� ���ͨ�ԣ�
������ A�����ݴ��������ԣ�pHΪС��7�����з����жϣ�
B�������������Ҫ�ɷ����������������ᷴӦ�����Ȼ�����ˮ�����з����жϣ�
C��������ʯ�Ҿ��м��ԣ����з����жϣ�
D������Ũ���������ˮ�ԣ����з����жϣ�
��� �⣺A�����������ԣ�pHΪС��7����pH��ֽ��ô�����Һ��pH������Ϊ9����ѡ��˵������
B���������Ҫ�ɷ����������������ᷴӦ�����Ȼ�����ˮ����ѡ��˵����ȷ��
C����ʯ�Ҿ��м��ԣ�������ʯ�Ҹ���������������ѡ��˵����ȷ��
D��Ũ���������ˮ�ԣ����������������ѡ��˵����ȷ��
��ѡ��A��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����������������;����ȷ�����Ĺؼ���
2.��2015•���ݣ�����û�������кͷ�Ӧԭ������
A�����ú�������þ��ҩ���������θ�����֢
B������ʯ�Ҹ�����������
C���ó涣ҧ��Ϳ�Ϸ���ˮ���ɼ���ʹ��
D������ʯ���������
�⣺A��������þ��θҺ�е����ᷴӦ�����Ȼ�þ��ˮ������ͼӦ�����κ�ˮ�ķ�Ӧ�����������кͷ�Ӧԭ������ѡ�����
B������ʯ�Ҹ�����������������ʯ���������е��ᷴӦ������ͼӦ�����κ�ˮ�ķ�Ӧ�����������кͷ�Ӧԭ������ѡ�����
C���ó涣ҧ��Ϳ�Ϸ���ˮ���ɼ���ʹ�������ó���ڵ��������ķ�Ӧ�����������кͷ�Ӧԭ������ѡ�����
D������ʯ���������������ʯ����ˮ��Ӧ�����������ƣ����������֮�������κ�ˮ�ķ�Ӧ��û�������кͷ�Ӧԭ������ѡ����ȷ��
��ѡ��D
3.��2015•���������������У����ڼ���ʳ����ǣ���
ѡ�� A B C D
ʳ�� ƻ��֭ ����֭ ţ�� ������
pH 2.9��3.3 3.5��4.5 6.3��6.6 7.6��8.0
A�� A B�� B C�� C D�� D
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ��ݴ˽��з����жϣ�
��� �⣺A��ƻ��֭��pHΪ2.9��3.3��С��7�������ԣ���������ʳ���ѡ�����
B������֭��pHΪ3.5��4.5��С��7�������ԣ���������ʳ���ѡ�����
C��ţ�̵�pHΪ6.3��6.6��С��7�������ԣ���������ʳ���ѡ�����
D���������pHΪ7.6��8.0������7���Լ��ԣ����ڼ���ʳ���ѡ����ȷ��
��ѡ��D��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ����Ĺؼ���
4.��2015•��������������¶���ڿ����У�������ѧ�仯��ʹ�������ӵ��ǣ�������
�� A�� Ũ���� B�� �ռ� C�� Ũ���� D�� ˫��ˮ
���㣺 �����г�������ε����������ʱ仯�����淨��.
ר�⣺ ���ʵı仯�����ʣ�
������ ����¶���ڿ����У�������ѧ��Ӧ�������ӣ�Ҳ����������еijɷַ����˻�ѧ��Ӧ���������µ����ʣ��ݴ˸��ݳ������ʵĻ�ѧ���ʽ��з����жϣ�
��� �⣺A��Ũ���������ˮ�ԣ������ڿ����л����տ����е�ˮ�֣�ʹ���������ӣ����������������仯����ѡ�����
B���ռ����������Ƶ��׳ƣ����ڷ����ڿ����У���������еĶ�����̼������ѧ��Ӧ����̼���ƺ�ˮ�������˻�ѧ��Ӧ�����������ӣ���ѡ����ȷ��
C��Ũ������лӷ��ԣ���ʹ���������٣���ѡ�����
D��˫��ˮ�������ֽܷ����������¶���ڿ����У���ʹ���������٣���ѡ�����
��ѡ��B��
������ �����ѶȲ�������ҩƷ�ڿ����е������仯�����лӷ��ԡ�������ˮ�ԡ���������еijɷַ�����ѧ��Ӧ�����ͣ�����ȷ��������Ĺؼ���
5.��2015•�������������������ʣ��Լ��Ե��ǣ�������
�� A�� ����ˮ��pH=10�� B�� ����֭��pH=2�� C�� ����ˮ��pH=7�� D�� ���ͣ�pH=5��
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��.
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ����з����жϣ�
��� �⣺A������ˮ��pHΪ10������7���Լ��ԣ���ѡ����ȷ��
B������֭��pHΪ2��С��7�������ԣ���ѡ�����
C������ˮ��pHΪ7�������ԣ���ѡ�����
D�����͵�pHΪ5��С��7�������ԣ���ѡ�����
��ѡ��A��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ��������Ĺؼ���
6.��2015•���ݣ��±��ǽ���������һЩҺ�����pH�����г����Ե��ǣ�������
|
θҺ |
��֭ |
Ѫ�� |
��Һ |
|
0.9��1.5 |
7.1��7.3 |
7.35��7.45 |
7.5��8.0 |
�� A�� θҺ B�� ��֭ C�� Ѫ�� D�� ��Һ
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��.
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ��ݴ˽��з����жϣ�
��� �⣺A��θҺpHΪ0.9��1.5��С��7�������ԣ���ѡ����ȷ��
B����֭��pHΪ7.1��7.3������7���Լ��ԣ���ѡ�����
C��Ѫ����pHΪ7.35��7.45������7���Լ��ԣ���ѡ�����
D����Һ��pHΪ7.5��8.0������7���Լ��ԣ���ѡ�����
��ѡ��A��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ��������Ĺؼ���
7.��2015•�������±��Ǽ��ֳ������ʵ�pH�������Լ��Ե��ǣ�������
|
���� |
ʳ�� |
����֭ |
����� |
��ľ��ˮ |
|
PH |
2.5 |
3.8 |
1.7 |
10.6 |
�� A�� ʳ�� B�� ����֭ C�� ����� D�� ��ľ��ˮ
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��.
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ����з����жϣ�
��� �⣺A��ʳ��pHΪ2.5��С��7�������ԣ���ѡ�����
B������֭��pHΪ3.8��С��7�������ԣ���ѡ�����
C��������pHΪ1.7��С��7�������ԣ���ѡ�����
D����ľ��ˮpHΪ10.6������7���Լ��ԣ���ѡ����ȷ��
��ѡ��D��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ��������Ĺؼ���
8.��2015•���ޣ�ȡһ��ֽ�����ȼ�����10����ɫʯ����Һ��װ�벣�����У�Ȼ��Ӳ����ܵ�����ͬʱ����ֱ�պ��Ũ��ˮ��Ũ���������Ѹ�ٷ�����˹ܿڣ��ܿ�ɹ۲쵽�����а��̲�������������ʧ�ɹ۲쵽��ͼ��ʾ������
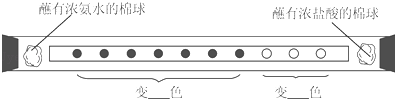
������˵������ȷ���ǣ�������
�� A�� ��ˮ�����ᶼ�����ӷ�������
�� B�� �ù�����û�л�ѧ��Ӧ����
�� C�� ����������ӵ��˶����ʶ���ͬ
�� D�� ͼʾ�ڵ��ʾʯ����Һ����˺�ɫ
���㣺 ��Ļ�ѧ���ʣ����ָʾ���������ʣ����ӵĶ�������ӵ����ԣ�.
ר�⣺ ��ѧ̽����
������ �������еķ����˶��Լ����ָʾ���������Һ�еı�ɫ��֪ʶ���з�����ɣ�
��� �⣺A�������а��̲���������Ϊ��ˮ�ӷ����İ���������ӷ������Ȼ��ⷴӦ�������Ȼ�淋�Ե�ʣ�˵����ˮ�����ᶼ�����ӷ������ʣ���ȷ��
B���ù����а������Ȼ��ⷴӦ�������Ȼ�泥������������ʣ������˻�ѧ�仯����ȷ��
C����ͼ���Կ�������ˮ��߱�ɫ�ĵ�����7�Σ�Ũ������ߵĵ�����3�Σ��ʰ������˶����ʴ����Ȼ��⣬˵�����ӵ��˶����ʲ�ͬ������
D����ˮ�ʼ��ԣ���ʹʯ����Һ���������Ǻ�ɫ������
��ѡA��
������ ���⿼����dz�������ͼ�Ļӷ����Լ����ָʾ����ɫ��֪ʶ����ɴ��⣬�����������е�֪ʶ���У�
9.��2015•���ޣ������й�˵���в���ȷ���ǣ�������
�� A�� ����Һ�ж�����H+�����������ƵĻ�ѧ����
�� B�� �ᡢ����ˮ��Һ�ж��ɽ�������������
�� C�� ��ʵ���ң�����Ũ����������ijЩ����
�� D�� ҽ���ϵ�������ˮ��0.9%�Ĵ�����Һ
���㣺 ��Ļ�ѧ���ʣ�Ũ��������ʼ�Ũ�����ϡ�ͣ��Ȼ���������ᴿ��.
ר�⣺ �������� ���ͨ�ԣ��������� ��ѧ���ϣ�
������ A��������Ķ�����з�����
B�������ᡢ��Ķ�����з�����
C������Ũ���������ˮ�Խ��з�����
D������ҽ���ϵ�������ˮ��0.9%���Ȼ�����Һ���з�����
��� �⣺A����ˮ��Һ�е������������ȫ���������ӵĻ��������ᣬ��A��ȷ��
B����ˮ��Һ�е������������ȫ���������ӵĻ��������ᣬ�������������ȫ�������������ӵĻ�����Ǽ��B��ȷ��
C��Ũ���������ˮ�ԣ���ʵ���ң�����������ijЩ���壬��C��ȷ��
D��ҽ���ϵ�������ˮ��0.9%���Ȼ�����Һ����D����
��ѡ��D��
������ ������Ҫ������һЩ����֪ʶ�ļ��䣬�ѶȲ���ֻҪ��ǿ���伴�ɽ��
������ѡ����
1.��2015•�������ڵ��з�̪��Һ��ϡ�����У���μ�������������Һ��ֱ����Һ�Ժ�ɫ��
��1����ʱ��Һ��pH�����ڡ�7����������������С������������������
��2��д����ʵ���з�Ӧ�Ļ�ѧ����ʽ����H2SO4+2NaOH=Na2SO4+2H2O����
���㣺 �кͷ�Ӧ����Ӧ�ã���Һ���������pHֵ�Ĺ�ϵ����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��.
ר�⣺ �������� ���ͨ�ԣ�
������ ��1������Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�
��2�������кͷ�Ӧ�Ķ����������ϻ�ѧ����ʽ��д�����ǣ�
��� �⣺��1���ڵ��з�̪��Һ��ϡ�����У���μ�������������Һ��ֱ����Һ�Ժ�ɫ��˵����Һ�Լ��ԣ�����pH����7��
��2���������ƺ����ᷴӦ���������ƺ�ˮ��������Ӧ�Ļ�ѧ����ʽ��H2SO4+2NaOH=Na2SO4+2H2O��
�ʴ�Ϊ��, , ��1�����ڣ�2��H2SO4+2NaOH=Na2SO4+2H2O
������ ���⿼��������кͷ�Ӧʱ��ҺPH�ı仯�Լ�����ʽ����д����ɴ��⣬�����������е�֪ʶ�Լ�ͼʾ���У�
2.��2015•������ij��ͬѧ����������Һ��ϡ��������кͷ�Ӧʵ�飺
��1����ͬѧʵ�������ͼ��
���ձ��м���Լ5mL����������Һ�����뼸����ɫ��̪��Һ����ʱ��Һ�����졡ɫ��
�����õιܵ���һ������ϡ���ᣬ���ò����������衡��������ҺΪ��ɫ�����Ǽ�ͬѧ�ó�����ǡ���к͵Ľ��ۣ���Ӧ�Ļ�ѧ����ʽΪ��NaOH+HCl=NaCl+H2O����
��2����ͬѧ�Լ�ͬѧ�Ľ�����������������Է�Ӧ����Һ�е����ʳɷֽ���̽����
��ʵ��̽����
��Ӧ����Һ�е�������ʲô��
����һ��ֻ��NaCl
�������NaCl��HCl
��������NaCl��NaOH
���ϲ����У�����ò���������������������
Ϊ����֤�������ֲ��룬��ͬѧ�������ʵ�鷽����
|
ʵ����� |
ʵ������ |
ʵ����� |
|
ȡ������Ӧ�����Һ���Թ��е���Na2CO3��Һ |
�������ݲ����� |
��������� |
����˼������
ʵ�������Һ����������ȷ������B��������ţ���
A��������ˮ�� B�������Һ�� C������ʵ���ң�

���㣺 ʵ��̽�����ʵ���ɳɷ��Լ���������Ļ�ѧ���ʣ���Ļ�ѧ���ʣ��кͷ�Ӧ����Ӧ�ã���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��.
ר�⣺ ��ѧ̽����
������ ��1����������������Һ�Լ��ԣ���ʹ��̪���ɫ��������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ���з�����
��2����ʵ��̽����������ҺΪ��ɫ��˵����Һ���Լ��Խ��з�����
���������̼���Ʒ�Ӧ�������Ȼ��ơ�ˮ�Ͷ�����̼���з�����
����˼����������ʵ����ʣ��ҩƷ�Ĵ����������з�����
��� �⣺��1������������Һ�Լ��ԣ���ʹ��̪���ɫ�������õιܵ���һ������ϡ���ᣬ���ò��������裬������ҺΪ��ɫ��������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ����ѧ����ʽΪ��NaOH+HCl=NaCl+H2O��
��2����ʵ��̽������ҺΪ��ɫ��˵����Һ���Լ��ԣ����Բ�������������
�����̼���Ʒ�Ӧ�������Ȼ��ơ�ˮ�Ͷ�����̼������
|
ʵ����� |
ʵ������ |
ʵ����� |
|
ȡ������Ӧ�����Һ���Թ��е���Na2CO3��Һ |
�������ݲ����� |
��������� |
����˼������ʵ����ʣ��ҩƷ���ܵ�����ˮ����Ҳ���ܴ���ʵ���ң�Ӧ�ý���Һ�����Һ���ڣ���ѡ��B��
�ʴ�Ϊ����1���죬���裬NaOH+HCl=NaCl+H2O��
��2����ʵ��̽������������
����˼������B��
������ Ҫ�����������Ŀ�����ȣ�Ҫ���������кͷ�Ӧ����Ӧ�õ����֪ʶ��Ȼ����������ʵ�顢�����龰��ͼ����Ϣ�ȣ������ѧ�����֪ʶ�ͼ��ܣ�ϸ�µط������Ⲣϸ�ĵ�̽��������������ĿҪ����������ѡ����ɣ�
3.��2015•���ݣ�������ˮƫ���ԣ�pHԼΪ5.6��������Ϊ�����е� A��������ˮ��Ե�ʣ�������ָpHС��5.6�Ľ�ˮ����Ҫ������Ϊ�ŷŵ���������͵����������������ת�����ɵģ������ķ�Ӧ��Ҫ�У�
��SO2+H2O�TH2SO3 ��2H2SO3+O2�T2H2SO4
��2NO+O2�T2NO2�����٣� ��3NO2+H2O�T2HNO3+NO
��ش������й����⣺
��1��A����Ļ�ѧʽΪ��CO2����
��2�������ĸ���ѧ��Ӧ�е����������У�����������������֣�
��3����������������Ӧ��֪��NO2�еĵ�Ԫ����������HNO3����д��ѧʽ��������ʽ���ڣ�
���㣺 ����IJ�����Σ�������Σ�������������ᡢ����ε��б�.
ר�⣺ ��ѧ�뻷��������
������ ������ˮƫ���ԣ�pHԼΪ5.6��������Ϊ�����еĶ�����̼��ˮ��Ӧ����̼���Ե�ʣ������pHС��5.6��ԭ������ˮ���ܽ��������������������ʱ�������������ᡢ�����ǿ�ᣬ��Һ���Խ�ǿ�����£��ݽ���йص����⣮
��� �⣺��1��������ˮƫ���ԣ�pHԼΪ5.6��������Ϊ�����еĶ�����̼��ˮ��Ӧ����̼�ᣬ����A�Ļ�ѧʽ�ǣ�CO2��
��2������ɷ����ķ�Ӧ��֪�������ĸ���ѧ��Ӧ�е����������У����������H2SO3��H2SO4��HNO3���֣�
��3���ɢۡ���������Ӧ��֪��NO2�еĵ�Ԫ��������HNO3������ʽ���ڣ�
�ʴ�Ϊ����1��CO2����2��������3��HNO3��
������ ���⿼��������ij������ʺ������ȣ��ѶȲ���ע����ۣ�
4.��2015•�żҽ磩�ڳ���CO2�������������м��������NaOH��Һ���ڣ������������������Ҫԭ���ǣ�CO2��NaOH��Һ�����˻�ѧ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ����CO2+2NaOH=Na2CO3+H2O����һ��������������ֹ�����ԭ���ǣ�Al��NaOH��Һ��Ӧ������H2��ͬʱ��ƫ�����ƣ���ѧʽΪ��NaAlO2�����ɣ�����һ�����У�����������ʹ�������ڵ�ѹǿ���Ӷ�ʹ�������������¹�����д��Al��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ����2A1+2NaOH+2H2O�T2NaAlO2+3H2�������˷�Ӧ�������ڡ��û���Ӧ����������������������������
���㣺 ��Ļ�ѧ���ʣ���Ӧ���͵��ж�����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ���ݶ�����̼�ܺ��������Ʒ�Ӧ����̼���ƺ�ˮ����Ŀ��Ϣ���ṩ�ķ�Ӧ��������Ӧ�������������غ㶨�ɿ�����д��Ӧ�Ļ�ѧ����ʽ���жϷ�Ӧ���ͣ�
��� �⣺�ڳ���CO2�������������м������NaOH��Һ���ڣ��������������ԭ����C02��������NaOH��Һ��Ӧ�������գ�ʹ������ѹ��С����Ӧ�ķ���ʽΪ��CO2+2NaOH=Na2CO3+H2O��һ����������ֹ�����Al��NaOH��Һ��Ӧ����H2��NaAlO2���û�ѧ����ʽΪ��2A1+2NaOH+2H2O�T2NaAlO2+3H2�����÷�Ӧ�ķ�Ӧ�������ֻ������һ�ֵ��ʣ���˲������û���Ӧ��
���CO2+2NaOH=Na2CO3+H2O��2A1+2NaOH+2H2O�T2NaAlO2+3H2���������ڣ�
������ ���⿼������������ı仯����ѹǿ�ı仯���Ӷ�������һϵ�е���������ѧ����ȡ��Ϣ����д����ʽ��������
5.��2015•���ޣ����ᣨCH3COOH����һ�ֳ������ᣬ�������ͨ�ԣ����磺����������������Һ��Ӧ���ɴ����ƺ�ˮ����ѧ����ʽΪ��CH3COOH+NaOH=CH3COONa+H2O��
��1��������������������һ����Ҳ��һ�ֳ����ļ���м��ͨ�ԣ���д������������������Һ�����кͷ�Ӧ���ɵ��εĻ�ѧʽ��CH3COOK����
��2������������һ����������ý�����Ӧ������������д�����������п��Ӧ�Ļ�ѧ����ʽ��2CH3COOH+Zn=��CH3COO��2Zn+H2������
���㣺 ��������ʼ�����ĺ����ⶨ����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��.
ר�⣺ �������� ���ͨ�ԣ�
������ ��1������������������Һ�����кͷ�Ӧ���ɴ���غ�ˮ��д������صĻ�ѧʽ���ɣ�
��2�����ݴ���������һ����������ý�����Ӧ�������������������п��Ӧ���ɴ���п����������Ӧ�Ļ�ѧ����ʽ���ɣ�
��� �⣺��1��CH3COONa����Ԫ����+1�ۣ��������ԩ�1�ۣ�����������������Һ�����кͷ�Ӧ���ɴ���غ�ˮ����Ԫ����+1�ۣ�������ԩ�1�ۣ��仯ѧʽΪ��CH3COOK��
��2������������һ����������ý�����Ӧ�������������������п��Ӧ���ɴ���п����������Ӧ�Ļ�ѧ����ʽΪ��2CH3COOH+Zn=��CH3COO��2Zn+H2����
�ʴ�Ϊ����1��CH3COOK����2��2CH3COOH+Zn=��CH3COO��2Zn+H2����
������ �����ѶȲ���������Ļ�ѧ���ʣ�������ý����������������ȷ�Ӧ�����������������ȷ�����Ĺؼ���
6.��2015•���ޣ�������ѧ��֪ʶ�ش��������⣺
��1��pH��5.6�Ľ����Ϊ���꣮Ϊʲô�ѱ���Ϊ5.6��
��2����ѩͬѧ��п����ϡ��������ͼ��ʾ��װ������ȡ������һ��ʱ����������ݲ������ڽ��������������ݲ�������ԭ��ʱ����ѩͬѧ��Ϊ������п����ϡ���������˽Ӵ�������Ϊ��������ʲôԭ��
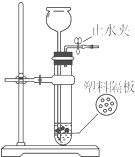
���㣺 ����IJ�����Σ�������Σ���������ȡ�ͼ��飮.
ר�⣺ �������� ���ͨ�ԣ�
������ ��1�����ݳ��³�ѹ�£�CO2������Һ��pH=5.6�������
��2��������ѹ�仯��ԭ���ش��粻©��������ˮ����������ѹ�仯���Ӷ���ʾһ��������
��� �⣺
��1�����³�ѹ�£�CO2������Һ��pH=5.6����������ˮ��pH��5.6������������Һ��˵��pHԽС������Խǿ����pH��5.6�Ľ����Ϊ���꣮
��2����ͼԭ���ǵ���Ҫ���Ƹ÷�Ӧֹͣʱ�����Լ��ϵ��ɼУ���ʱ���ɵ�����ͻ��Ƿ�Ӧ�����е�ѹǿ���Ӷ���Һ��ѹ�س���©�������չ�Һ���룬��Ӧֹͣ�������ɼ�ʱ������ͨ�������ų���Һ���½�����Һ�Ӵ�����Ӧ���У���һ��ʱ����������ݲ�����������ij�ַ�Ӧ���Ѿ�������ϣ�
�𰸣�
��1�����³�ѹ�£�CO2������Һ��pH=5.6����������ˮ��pH��5.6����
��2��ij�ַ�Ӧ���Ѿ�������ϣ�
������ ���⿼������֮��ķ�Ӧ��������Ҫ�ܸ��ݸ�װ�õ��ص����ʵ������
��2014�꣩
1.��2014•���£�����һЩҺ�������pH��Χ���£�����������ǿ���ǣ�������
�� A�� θҺ0.9��1.5 B�� ��֭7.1��7.3 C�� Ѫ��7.35��7.45 D�� ��Һ4.7��8.4
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ���pHԽС������Խǿ������Һ��pH����7ʱ���ʼ��ԣ���pHԽ����Խǿ���ݴ˽��з����жϼ��ɣ�
��� �⣺A��θҺ��pHΪ0.9��1.5��С��7�������ԣ�
B����֭��pHΪ7.1��7.3������7���Լ��ԣ�
C��ѪҺ��pHΪ7.35��7.45������7���Լ��ԣ�
D����Һ��pHΪ4.7��8.4�����������ԡ����ԡ����ԣ�
���ݵ���Һ��pHС��7ʱ�������ԣ���pHԽС������Խǿ��θҺ��pH��С��������ǿ��
��ѡA��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ����Ĺؼ���
2.��2014•���£�����ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һ����ͼ������������ȷ���ǣ�������

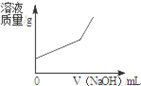
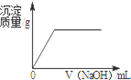
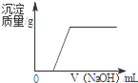
A�� B�� C�� D��
���㣺 ��Ļ�ѧ���ʣ���Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ����ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һʱ�����������Ⱥ�ϡ���ᷴӦ�����Ȼ��ƺ�ˮ����ϡ������ȫ��Ӧ�����������ٺ��Ȼ�ͭ��Ӧ����������ͭ�������Ȼ��ƣ�
��� �⣺A������ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һʱ�������������ƺ�ϡ���ᷴӦ�Ľ��У���Һ�����Լ�����pH���ߣ���ϡ������Ȼ�ͭ����ȫ��Ӧ�����μ�����������Һʱ����Һ�Լ��ԣ�pH����7����ѡ����������ȷ��
B������ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һʱ���������ƺ�ϡ���ᷴӦʱ����Һ�������ӣ����������ƺ��Ȼ�ͭ��Ӧʱ����Һ������С�����Ȼ�ͭ��ȫ��Ӧ�����μ�����������Һʱ����Һ��������ѡ����������ȷ��
C������ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һʱ�����������Ⱥ�ϡ���ᷴӦ����ʼ��������������ѡ����������ȷ��
D������ϡ������Ȼ�ͭ�Ļ����Һ�еμ�NaOH��Һʱ�����������Ⱥ�ϡ���ᷴӦ����ʼ��������������ϡ������ȫ��Ӧ���������ƺ��Ȼ�ͭ��Ӧ�������������Ȼ�ͭ��ȫ��Ӧ���ٲ�����������ѡ��������ȷ��
��ѡ��D��
������ ʵ������������֮������õ����ڱ��֣����Ҫѧ�����ʵ�顢�۲�ʵ�顢����ʵ�飬Ϊ��ʾ����֮������õ�ʵ�ʵ춨������
3.��2014•���ݣ�һЩʳ�����phֵ���£�ţ��6.4��ƻ��֭3.1��������7.8������֭4.0������������ǿ���ǣ�������
�� A�� ƻ��֭ B�� ������ C�� ţ�� D�� ����֭
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ pHԽС������Խǿ�����⽫����Ե�֪ʶ�������ճ������У�ʹѧ����һ����ʶ����ѧ֪ʶ���˵����彡���йأ�
��� �⣺����Һ��pH����7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH��7ʱ����pHֵԽС����Խǿ��
ƻ��֭��pHС��7��������С��������ǿ��
��ѡA��
������ �����Ҫ���������Һ������Ժ���ҺPH��С֮��Ĺ�ϵ��ֻ���������ܶ���ط��������������ȷ���жϣ�
4.��2014•¦�ף������Ǽ�ͥ�г��õ�ϴ�Ӽ�����pH�����������Ե��ǣ�������
�� A�� ϴ������pH=8�� B�� ����������pH=1��
C�� ϴ��Һ��pH=10�� D�� ����������pH=13��
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��.
ר�⣺ �������� ���ͨ�ԣ�
������ �������е�֪ʶ���з�����pHС��7����Һ�����ԣ�pH����7����Һ�ʼ��ԣ��ݴ˽��
��� �⣺A��ϴ������pH=8�����ʼ��ԣ�����
B������������pH=1���������ԣ���ȷ��
C��ϴ��Һ��pH=10�����ʼ��ԣ�����
D������������pH=13�����ʼ��ԣ�����
��ѡB��
������ ���⿼������Һ���������pH�Ĺ�ϵ����ɴ��⣬�����������е�֪ʶ���У�
5.��2014•¦�ף����ձ�����μ���X��Һ��������ͼ�ף������ɳ���������������������꣩�����X��Һ�������������꣩��ϵ������ͼ�ҵ��ǣ�������
|
|
�ձ��е����� |
X��Һ |
|
A |
ϡ�����ϡ���� |
�Ȼ�����Һ |
|
B |
ϡ���������ͭ��Һ |
����������Һ |
|
C |
����ʯ��ˮ |
̼������Һ |
|
D |
̼��������Һ |
ϡ���� |
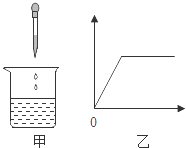
���㣺 ��Ļ�ѧ���ʣ���Ļ�ѧ���ʣ�.
ר�⣺ Ԫ�ػ�����֪ʶ�ͣ�
������ ��ͼ�п�֪������֮�������ʱ����ʼ�Ͳ������������壬�ݴ˸��ݸ�����֮��ķ�Ӧ������з�����
��� �⣺A���Ȼ�����ϡ���ᷴӦ���ɵij������ᱵ������ϡ���ᣬ��ʼ�Ͳ�������������ͼ��
B�����������ܺ�����ͭ��Ӧ����������ͭ������������ͭ�ܺ����ᷴӦ�����Ȼ�ͭ��ˮ����ʼû�г������֣��������������ų��ֳ�����������ͼ��
C������ʯ��ˮ��̼������Һ��Ӧ����̼��Ƴ�������ʼ�Ͳ�������������ͼ��
D��̼��������Һ��ϡ���ᷴӦ���ɶ�����̼���壬��ʼ�Ͳ������壬����ͼ��
��ѡB��
������ �����Ҫ���ո������ʵ����ʷ�������ݣ�ֻ���������ܶ�ʵ������������ȷ���жϣ�
6.��2014•��������������¶���ڿ����У�һ��ʱ����������ӵ��ǣ�������
�� A�� ����ʯ B�� ˫��ˮ C�� Ũ���� D�� �ռ�
���㣺 �����г�������ε����������ʱ仯�����淨��
ר�⣺ ���ʵı仯�����ʣ�
������ ���ݳ������ʵ������ͻ�ѧ�������η������ɣ�����ʯ�ڿ�����������������仯��Ũ������лӷ��ԣ��ӷ����Ȼ������壬����Ҳ���٣��������ƹ����ڿ����лᳱ�Ⲣ�������̼��Ӧ�����������ӣ�
��� �⣺A������ʯ�ڿ�����������������仯���ʴ���
B��˫��ˮ�ڿ����л�ֽ��������������С���ʴ���
C��Ũ������лӷ��ԣ��ӷ����Ȼ������壬������С���ʴ���
D���ռ�����ڿ����лᳱ�Ⲣ�������̼��Ӧ�����������ӣ��ʶԣ�
��ѡ��D��
������ �����ǶԳ����������ʵĿ��飬������ص��Ƕ����������ڿ����еı仯������˽⣬�����������ʻ���֪ʶ�����⣮
7.��2014•������ijͬѧ���Ͳ˵ز������۷䵪���ˣ��۷�Ĵ�Һ�����ԣ�Ϊ�˼���ʹ���������˴�ͿĨ�������ǣ�������
A�� ţ�̣�pH��6�� B�� ƻ��֭��pH��3�� C�� ���ࣨpH��9�� D�� ��Ȫˮ��pH��7��
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�����Һ��pHС��7ʱ�������ԣ��������⣬�۷�Ĵ�Һ�����Եģ����������кͷ�Ӧ��ԭ����ͿĨ�Լ��Ե����ʣ�
��� �⣺��Ϊ�۷�Ĵ�Һ�����Եģ�Ϊ�˼���ʹ����Ӧ�������˴�ͿĨ�Լ��Ե����ʣ�
A��ţ�̵�pH��6��С��7�������ԣ���ѡ�����
B��ƻ��֭��pH��3��С��7�������ԣ���ѡ�����
C�������pH��9������7���Լ��ԣ���ѡ����ȷ��
D����Ȫˮ��pH��7�������ԣ���ѡ�����
��ѡ��C��
������ �����ѶȲ��������кͷ�Ӧ��ԭ������ҺpH��С֮��Ĺ�ϵ����ȷ�����Ĺؼ���
8.��2014•��̶��һЩʳ��Ľ���pH���±�������������ǿ�������ǣ�������
|
pH |
3.5��4.5 |
2.9��3.3 |
6.3��6.6 |
7.6��8.0 |
|
ʳ�� |
A������֭ |
B��ƻ��֭ |
C��ţ�� |
D�������� |
�� A�� ����֭ B�� ƻ��֭ C�� ţ�� D�� ������
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�����Һ��pHС��7ʱ�������ԣ�
����Һ��pHС��7ʱ������pH�ļ�С������ǿ��
��� �⣺�������pH����7���Լ��ԣ�����֭��ƻ��֭��ţ�̵����ʵ�pHС��7�������ԣ�����ƻ��֭��pH��С��������ǿ��
��ѡB��
������ �����Ҫ������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ��Ȼ���ٸ��ݾ������ʵ�ˮ��Һ������Խ��з������жϣ��Ӷ��ó���ȷ�Ľ��ۣ�
9.��2014•��̶��ʵ������п����ϡ���ᷴӦ��ȡ����������װ����ͼ��ʾ��������ע��ϡ���ᣬ����ϡ����δ�����п����ϰ��ϵ�п���Ӵ�������ʱ����ϡ����ɼӣ���������Һ�У������˴ӳ���©�����ӵ��ǣ�������
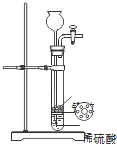
�� A�� ����������Һ B�� ̼������Һ C�� ��������Һ D�� ����ʯ��ˮ
���㣺 ��Ļ�ѧ���ʣ�
ר�⣺ �������� ���ͨ�ԣ�
������ �������ơ�̼���ƺ��������ƶ��ܹ���ϡ���ᷴӦ������Ӧ�����ʣ��Ӷ�����ϡ���
�����Ʋ��ܺ�ϡ���ᷴӦ��
��� �⣺A��ϡ������������Ʒ�Ӧ���������ƺ�ˮ�������������������Һ����Ӱ������������������˲����˼�������������Һ��
B��ϡ�����̼���Ʒ�Ӧ���������ơ�ˮ�Ͷ�����̼������Ӱ�������������������ܹ�ʹ���������к��ж�����̼����˲����˼���̼������Һ��
C��ϡ����������Ʋ��ܷ�Ӧ��������������Һʱ���ܹ�ʹϡ�����п�Ӵ����Ӷ�ʹ��Ӧ˳�����У���������˴ӳ���©�����ӵ�����������Һ��
D�����������ܺ�ϡ���ᷴӦ��������ƺ�ˮ������������ʯ��ˮ����Ӱ������������������˲����˼������ʯ��ˮ��
��ѡ��C��
������ �����һЩ���ƵĻ�ѧ���ʣ�������ʹʯ����Һ���ɫ���ܺ�ijЩ�������ʡ�ijЩ���������ijЩ�Ρ��Ӧ������Ӧ�����ʣ�
10.��2014•�żҽ磩����������һ�ֳ����ļ���������ǣ�������
�� A�� ����ʯ B�� ��ʯ�� C�� ʯ��ʯ D�� ��ʯ��
���㣺 ����������Ժ���;��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ��dz������ʵ����ơ���ѧʽ����������;�����������׳���ʯ�ҡ���ʯ�ң�
��� �⣺�������Ƶ��׳�����ʯ�һ���ʯ�ң���ʯ��Ϊ�����ƣ�ʯ��ʯ�ʹ���ʯ����Ҫ�ɷ���̼��ƣ���
��ѡB��
������ ������Ҫ����ѧ���Գ������ʵ����ơ���ѧʽ����������;��Ҫ�ܰ����ʵ��׳ƺ�ѧ����Ӧ������
11.��2014•���ޣ�������ѧ��֪ʶ�ش��������⣺
��1��Ϊʲô�Ϳ⡢��۳���Ҫ�Ͻ��̻�
��2��ij�¶��£���ѩͬѧ�ô������Ȼ��ƹ������ƺ�5%���Ȼ�����Һ����pH�ƣ���ȷ�ⶨ��ҺpH����������ø��Ȼ�����Һ��pH=6.5�����ǵó��Ȼ�����Һ�����ԵĽ��ۣ�����Ϊ��ѩͬѧ�Ľ����Ƿ���ȷ��������ȷ������Ҫ����ʲô�Ա�ʵ�飿
���㣺 ������ը�Ĵ�ʩ����Һ�����Ȳⶨ��
ר�⣺ ��ѧ�����������������ѧʵ�����������
������ ��1�����ݱ�ըָ��ȼ�������Ŀռ��ڼ����ȼ�գ��ͻ��ڶ�ʱ���ھۼ��������ȣ�ʹ��������Ѹ�����Ͷ�����ը������⣻
��2�������Ȼ�����Һ�������Dz���ȷ�Ľ��н��
��� �⣺��1����Ϊ��۳�������վ��Щ�ط��Ŀ����г����п�ȼ�ķ۳����ȼ�����壬�������������з�����ը��Σ�գ�����Ҫ�Ͻ��̻�
�ʴ�Ϊ����۳�������վ��Щ�ط��Ŀ����г����п�ȼ�ķ۳����ȼ�����壬�������������з�����ը��Σ�գ�����Ҫ�Ͻ��̻�
��2�������������Ȼ�����Һ�����ԣ�pH=7�����Բ�ø��Ȼ�����Һ��pH=6.5���ó��Ȼ�����Һ�����ԵĽ����Ǵ���ģ�����Ҫ�ⶨ�����Ȼ�����Һ����ˮ��pHֵ��
�ʴ�Ϊ������ȷ����Ҫ�ⶨ�����Ȼ�����Һ����ˮ��pHֵ��
������ ���⿼���˱�ը���й�֪ʶ�����������е�Ӧ���Լ���Һ��pHֵ�����ڻ���֪ʶ�Ŀ��飬�ѶȽ�С����
12��2014•���ݣ���ͼ��ij�о���ѧϰС�����CO2��NaOH��Һ��Ӧ��̽��ʵ��װ�ã�
���������ϡ�ˮ�ķе�������ѹǿ�йأ�����ѹǿС���е�ͣ�����ѹǿ�е�ߣ�
��ʵ��̽����ʵ�鲽�����£�
����������ͼ��ʾ����ƿAʢ��CO2���壬��ƿBʢ��96%���ϵ�δ���ڵ���ˮ���ձ��м���ͬ���¶ȵ���ˮ���𱣳���ƿB��ˮ�º㶨�����ã���
��������ȡ2֧ע������һ֧��ȡ20mLˮ����һ֧��ȡ20mLŨNaOH��Һ��
����������ע������20mLˮע����ƿA�У���۲죬��ƿB�е���ˮû�з��ڣ�
��������ȡ��ʢˮ��ע�������ٽ�ʢ20mLŨNaOH��Һ��ע����Ѹ�����ӵ���ƿA�ϣ�ע�����Һ�����۲쵽���Ե�����
��ش��������⣺
��1��ʵ�鿪ʼǰ������ͼ���Ӻ�װ�ã���ƿA��B���ձ���δʢװ���ʣ�����һ֧��ע�������ӵ���ƿA�ϣ���������������������������Ӻ����֣��۲�����Ƿ�λ�����������Ŀ���������װ�������ԡ���
��2����ƿA��CO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ����2NaOH+CO2�TNa2CO3+H2O����
��3����������ƿB�в�����������������ˮ���ڡ����������������ԭ������B����ѹ��С��ˮ�ķе㽵�͡���
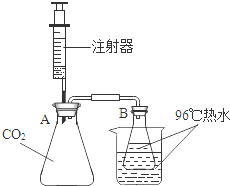
���㣺 ��Ļ�ѧ���ʣ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ��1�����ݼ��װ�������Եķ����������
��2��������̼���Ժ�����������Һ������Ӧ������̼���ƺ�ˮ��
��3������ѹԽСˮ�ķе�Խ�ͷ�����
��� �⣺��1����ע�������װ�õ������ԣ���������ƿ�м�������ˮ����û����©���¶ˣ�Ȼ��ע����C���ӵ�װ��E�ĵ��ܿڴ�����������ע����C�Ļ������۲쵽����©���¶�������ð����˵��װ�õ����������ã�
��2�����ڶ�����̼���Ժ�����������Һ������Ӧ������̼���Ƶ�ˮ���仯ѧ����ʽΪ��2NaOH+CO2�TNa2CO3+H2O��
��3��������������ƿA�е�CO2���巴Ӧ������̼���ƺ�ˮ��ʹƿ����ѹ��С��ˮ�ķе㽵�ͣ��ʽӽ����ڵ�ˮ�Ὺʼ���ڣ�
�ʴ�Ϊ����1�����װ�������ԣ���2��2NaOH+CO2�TNa2CO3+H2O����3��ˮ���ڣ�B����ѹ��С��ˮ�ķе㽵�ͣ�
������ ���⿼��֪ʶ�Ƚ�ȫ�棬�����˷�Ӧԭ���������Եļ�顢��ѹ��е�Ĺ�ϵ������
13.��2014•���ݣ�����ֲ�ﻨ��Ľ���Һ�������Ի������Һ������ֳ���ͬ����ɫ���ڻ�ѧʵ�����У����������ָʾ��������ȡ����ֲ�ﻨ��Ľ���Һ�ֱ����������Һ�У�ʵ���¼���±���
|
ֲ�����Һ |
ϡ������Һ |
�Ȼ�����Һ |
ϡ����������Һ |
|
���پ� |
��ɫ |
��ɫ |
��ɫ |
|
ǣţ�� |
��ɫ |
��ɫ |
��ɫ |
|
õ�廨 |
dz��ɫ |
dz��ɫ |
��ɫ |
��������ش��������⣺
��1�������������Һ�У����������ָʾ�����������پա���
��2������ǣţ������Һ���뵽ʳ���У���Һ������졡ɫ������õ�廨����Һ����ij��ɫ��Һ�У���Һ����ɫ�������Һ��pH������7����������������������=����
���㣺 ���ָʾ���������ʣ���Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ �������е�֪ʶ���з��������������Һ������ʾ��ͬ��ɫ�����ʿ��������ָʾ�������ݱ����ṩ����Ϣ���н�ɣ�
��� �⣺��1�����پյ�֭Һ��������Լ�������Һ�е���ɫһ�������������ָʾ����������پգ�
��2��ǣţ������Һ��������Һ��Ϊ��ɫ��õ�廨����Һ�ڼ�����Һ��Ϊ��ɫ��������Һ��pH����7������죬����
������ ���⿼������Һ���������pH�Ĺ�ϵ����ɴ��⣬�����������е�֪ʶ���У�
14.��2014•��̶����1��С�����ڵĻ�ѧ��ȤС��������������������Ϊ6%���Ȼ�����Һ80g�Ա�ʵ��
����Ҫ�Ȼ��Ƶ�����Ϊ��4.8�� g��
�����Ƹ���Һʱ����Ҫ�IJ����������ձ�������������ͷ�ιܺ�����Ͳ����
����������Ƶ���Һ��������������ƫ���ܵ�ԭ������B��������ĸ��ţ�
A������ʱ����������ǵ�������ͬ��ֽƬ
B��ȡˮʱ�����Ӷ���
C��װƿʱ����������Һ����
��2��װƿ��С�����Ǽ�ʱ���ϱ�ǩ�����º�һƿ�����ǩ��ϡ������Һ�����ˣ�Ϊ�����ֿ��������������������ʵ����ƣ�
������ѧ�������ڲ�ѡ�����ָʾ����pH��ֽ������£�ѡ���������ͬ���Լ����֣����������ָ���ʡ�������ᡢ��εȣ���
|
|
��ѡ�Լ� |
ʵ�������� |
|
����һ |
����� |
�������ݲ����������ᣬ�����ݲ��������Ȼ�����Һ�� |
|
������ |
��CuO�� |
����ʹCuO�ܽ⣬��Һ�����������ᣬ����������Ȼ�����Һ�� |
��������������С��ͬѧ��ʹ���˾ƾ��ƺͲ����������������Ͱ���������ɫ��Һ���ֿ����ˣ�����²�һ��������������Ҫ���������������жϷ��������ò������ֱ�պȡ������Ʒ���ھƾ��ƻ��������գ����������а�ɫ������ֵ�ԭ��Ʒ���Ȼ�����Һ��û�а�ɫ������ֵ�ԭ��Ʒ��ϡ���ᡡ��
���㣺 һ������������������Һ�����ƣ���Ļ�ѧ���ʣ��ᡢ��εļ���
ר�⣺ ���ʵļ����⣻��Һ����Һ���ܽ�ȣ�
������ ��1������������=��Һ���������������������
�ڸ������Ƹ���Һʱ����Ҫ�IJ����������
�����Ƶ���Һ��������������ƫ���ܵ�ԭ�������ʶ��˻��ܼ����˽��
��2��������Ҫ������ϡ������Ȼ�����Һ���й����ʼ���صķ�Ӧ��������������ȷ�����ʣ�
�ٻ�ѧ������Ҫ�Ǹ��ݷ����Ļ�ѧ�仯�е�����ͬ��ȷ����
������������Ҫ��ʹ���˾ƾ��ƺͲ����������������������ʵĻӷ��ԣ�
��� �⣺��1������Ҫ�Ȼ��Ƶ�����Ϊ��80g��6%=4.8g��
�����Ƹ���Һʱ����Ҫ�IJ����������ձ�������������ͷ�ιܺ���Ͳ��
��A������ʱ����������ǵ�������ͬ��ֽƬ��ʹ�Ȼ��Ƶ�����������ֵ���ˣ��������������ƫС��
B��ȡˮʱ�����Ӷ����������ˮ���ˣ��������������ƫ��
C��װƿʱ����������Һ����������Ӱ����������������
�ʴ�B�������⣻
��2����ѧ����Ҫ����ѡ�Լ��Dz�ͬ�������ģ�������ͬ���������ȷ����ͬ���ʣ��������������Ӧ�����Ȼ�����Һ���������Ӧ������������ͭ��Ӧ�õ���ɫ��Һ�����Ȼ�����Һ��������ͭ��Ӧ��
���������ӷ����ʿ����ò������ֱ�պȡ������Ʒ���ھƾ��ƻ��������գ����������а�ɫ������ֵ�ԭ��Ʒ����������Һ��û�а�ɫ������ֵ�ԭ��Ʒ��ϡ���ᣮ
�𰸣���1����4.8g ����Ͳ ��B
��2����
|
|
��ѡ�Լ� |
ʵ�������� |
|
����һ |
� |
�����ݲ����������ᣬ�����ݲ��������Ȼ�����Һ |
|
������ |
CuO |
��ʹCuO�ܽ⣬��Һ�����������ᣬ����������Ȼ�����Һ |
���ò������ֱ�պȡ������Ʒ���ھƾ��ƻ��������գ����������а�ɫ������ֵ�ԭ��Ʒ���Ȼ�����Һ��û�а�ɫ������ֵ�ԭ��Ʒ��ϡ���ᣮ
������ Ӧע�ز�ͬ����֮��������ϵIJ��죬��ƺ�����ʵ����ͨ���������ֻ�������ʣ��������нϴ��˼ά�ռ䣬�����ж��֣����ᳫһ���𰸣�
15.��2014•��������������ᶼ��ʵ���ҳ��õ��ᣬ�������������Ƶ����ʣ�
��1��ˮ��Һ��pH����С�ڡ�7����������������С����������������
��2�����ܳ�ȥ���⣮���������������ϡ�����У��ɿ�����������ʧ����Һ��ɫ��Ϊ����ɫ����
��3�����������кͷ�Ӧ����д���������������Ʒ�Ӧ�Ļ�ѧ����ʽ��2NaOH+H2SO4=Na2SO4+2H2O����
���㣺 ��Ļ�ѧ���ʣ���Һ���������pHֵ�Ĺ�ϵ����д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
ר�⣺ �������� ���ͨ�ԣ�
������ ��1������Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�
��2���������Ҫ�ɷ����������������ᷴӦ�����Ȼ�����ˮ���ݴ˽��з������
��3���������������Ʒ�Ӧ���������ƺ�ˮ��д����Ӧ�Ļ�ѧ����ʽ���ɣ�
��� �⣺��1�����������������ԣ�ˮ��Һ��pH��С��7��
��2���������Ҫ�ɷ����������������ᷴӦ�����Ȼ�����ˮ���ɿ�����������ʧ����Һ��ɫ��Ϊ��ɫ��
��3���������������Ʒ�Ӧ���������ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��2NaOH+H2SO4=Na2SO4+2H2O��
�ʴ�Ϊ����1��С�ڣ���2����ɫ����3��2NaOH+H2SO4=Na2SO4+2H2O��
������ �����ѶȲ���������Ļ�ѧ���ʡ���Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ����Ĺؼ�����
16.��2014•���ݣ���ͼ��ijͬѧѧϰ���������ƵĻ�ѧ���ʺ���Ƶ�֪ʶ����ͼ������A��B��C�ֱ��ʾ��ͬ���Ļ������֪A��һ�������Σ�����Һ����ɫ��B��������𣬡�������ʾ����������֮�������Ӧ��
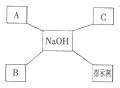
��1�������ʷ��࣬C�������ᡡ�������������ᡱ��������Ρ�����
��2��д��A��B�Ļ�ѧʽ��A��CuSO4����B��CO2����
��3��д��C��һ��������NaOH��Ӧ�Ļ�ѧ����ʽ��HCl+NaOH=NaCl+H2O����
��4��NaOH��A��Ӧ��ʵ��������������ɫ�������ɡ���
���㣺 ��Ļ�ѧ���ʣ�������������ᡢ����ε��б𣻻�ѧʽ����д�����壻��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ���ݼ�Ļ�ѧ���ʣ�������ǽ���������ᡢ�εȷ�Ӧ��A��B��C�ֱ��ʾ��ͬ���Ļ������֪A��һ�������Σ�����Һ����ɫ����AΪ����ͭ��Һ��B�����������BΪ������̼���ݴ˽��з������
��� �⣺��1���ɼ�Ļ�ѧ���ʣ�������ǽ���������ᡢ�εȷ�Ӧ��A��B��C�ֱ��ʾ��ͬ���Ļ������֪A��һ�������Σ�����Һ����ɫ����AΪ����ͭ��Һ��B�����������BΪ������̼��Ϊ�ǽ����������C�����ᣬ�������кͷ�Ӧ��
��2��AΪ����ͭ��Һ��BΪ������̼���仯ѧʽ�ֱ���CuSO4��CO2��
��3��CΪ�ᣬ������������������Һ��Ӧ�����Ȼ��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��HCl+NaOH=NaCl+H2O���������ɣ���
��4��NaOH������ͭ��Һ����������ͭ��ɫ��������������Һ����۲쵽����ɫ�������ɣ�
�ʴ�Ϊ����1�����2��CuSO4��CO2����3��HCl+NaOH=NaCl+H2O����4������ɫ�������ɣ�
������ �����ѶȲ������ռ�Ļ�ѧ���ʡ���ѧ����ʽ����д�������������������ȷ�����Ĺؼ���
��2013�꣩
1.��2013•�����������й�ʵ�������������ȷ���ǣ�������
�� A�� ������������ȼ�ղ��������İ���
�� B�� ��ϡ�����еμ�������ɫ��ʯ����Һ����Һ����ɫ����ɫ�����ɫ
�� C�� ���ڿ�����ȼ�ղ�������������ɫ����
�� D�� ��ʢ��Ũ������Լ�ƿƿ�ǣ�ƿ���Ϸ����ִ�������
���㣺 ������̼���ס����������ʵķ�Ӧ����Ũ��������ʼ�Ũ�����ϡ�ͣ���Ļ�ѧ���ʣ�
ר�⣺ ��Ͽα�֪ʶ����Ϣ��
������ A��������������ȼ�������ɴ����İ�ɫ�������������ף�������������������ɢ���ܲ��������İ��̣�
B�������Ե���Һ��ʹʯ����Һ���ɫ��
C�����ڿ�����ȼ��ʱ�ܷ�������ɫ�Ļ��棻
D��Ũ���������ˮ�ԣ������лӷ��ԣ�
��� �⣺A��������������ȼ�ղ��������İ��̣���ѡ����ȷ��
B����ϡ�����еμ�������ɫ��ʯ����Һ����Һ����ɫ����ɫ��ɺ�ɫ����ѡ�����
C�����ڿ�����ȼ�ղ��ܲ�������������ɫ���森��ѡ�����
D����ʢ��Ũ������Լ�ƿƿ�ǣ�ƿ���Ϸ����ܳ��ִ�����������ΪŨ������лӷ��ԣ���ѡ�����
��ѡA��
������ ������Ҫ�����ȼ��ȼ��ʱ��ʵ�������ʱӦ�ôӻ��桢�⡢��������Һ��ɫ�仯�ȷ�����з������жϣ��Ӷ��ó���ȷ�Ľ��ۣ�
2.��2013•¦�ף������ʵ���ɽǶȽ�����������ƻ�ѧ���ʵ�ԭ���ǣ�������
�� A�� �ᶼ����ˮ�е����H+ B�� �ᶼ�������
�� C�� ���ж��������� D�� ���ж�������Ԫ��
���㣺 ��Ļ�ѧ���ʣ�
ר�⣺ �������� ���ͨ�ԣ�
������ �������ǵ���ʱ������������ȫ���������ӵĻ�����ݴ��Է����жϼ��ɣ�
��� �⣺A������Һ�������ƻ�ѧ���ʵ�ԭ������ˮ��Һ�ж��ܵ���������ӣ���ѡ����ȷ��
B������Һ�������ƻ�ѧ���ʵ�ԭ������ˮ��Һ�ж��ܵ���������ӣ������Ǻ����������ѡ�����
C������Һ�������ƻ�ѧ���ʵ�ԭ������ˮ��Һ�ж��ܵ���������ӣ����в�����������ѡ�����
D������Һ�������ƻ�ѧ���ʵ�ԭ������ˮ��Һ�ж��ܵ���������ӣ����������ж�������Ԫ�أ���ѡ�����
��ѡA��
������ �����ѶȲ�����Ҫ��������������ƻ�ѧ���ʵ�ԭ�Ӷ�����ѧ�������ͨ�Ե����⣮
3.��2013•������������Һ���Լ��ԣ�pH >7�����ǣ�D ��
A. ϡ���� B. ������Һ C. ϡ���� D. �ռ���Һ
4.��2013•������������һЩҺ��pH�����£���Һ��6.6��7.1����θҺ��0.9��1.5����Ѫ����7.35��7.45������Һ��4.7��8.4��������������ǿ���ǣ�������
�� A�� ��Һ B�� θҺ C�� Ѫ�� D����Һ
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ ��Ͽα�֪ʶ����Ϣ��
������ ����Һ��pH����7ʱ�������ԣ�����Һ��pHС��7ʱ�������ԣ���pHԽС������Խǿ������Һ��pH����7ʱ���ʼ��ԣ���pHԽ����Խǿ���ݴ˽��з����жϼ��ɣ�
��� �⣺A����Һ��pHΪ6.6��7.1�����������ԡ����Ի���ԣ�
B��θҺ��pHΪ0.9��1.5��С��7�������ԣ�
C��Ѫ����pHΪ7.35��7.45������7���Լ��ԣ�
D����Һ��pHΪ4.7��8.4�����������ԡ����Ի���ԣ�
���ݵ���Һ��pHС��7ʱ�������ԣ���pHԽС������Խǿ��θҺ��pH��С��������ǿ��
��ѡB��
������ �����ѶȲ���������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ȷ����Ĺؼ���
5.��2013•��������ͼ��Բ�ཻ��������������������֮�����Ӧ��ʾ��ͼ�����жԷ�Ӧ�����˵���У�������ǣ�������
�� A�� a���γ�dz��ɫ��Һ B�� b���γɴ�������
�� C�� c����Ӧ���� D�� d����Һ�ʺ�ɫ
���㣺 ��Ļ�ѧ���ʣ���Ļ�ѧ���ʣ�
ר�⣺ �������� ���ͨ�ԣ������ļ� ���ͨ�ԣ�
������ A��a��Ϊ��������ķ�Ӧ���÷�Ӧ�������������Ȼ����������Ծݴ˽��
B��b��Ϊ̼������Һ��ϡ����ķ�Ӧ���÷�Ӧ�����˶�����̼���壬���Ծݴ˽��
C��c��Ϊ�������ƺ�����ķ�Ӧ���÷�ӦΪ�кͷ�Ӧ���Ƿ��ȷ�Ӧ�����Ծݴ˽����⣻
D��ʯ�����������������죬���Ծݴ˽����⣮
��� �⣺A��a��Ϊ��������ķ�Ӧ���÷�Ӧ�������������Ȼ������������Ȼ�������ҺΪdz��ɫ��Һ�����Կ��Թ۲쵽��Һ��Ϊdz��ɫ����A������ȷ��
B��b��Ϊ̼������Һ��ϡ����ķ�Ӧ���÷�Ӧ�����˶�����̼���壬���Կ��Թ۲쵽b�������˴��������ݣ���B������ȷ��
C��c��Ϊ�������ƺ�����ķ�Ӧ���÷�ӦΪ�кͷ�Ӧ���Ƿ��ȷ�Ӧ����C������ȷ��
D��ʯ�����������������죬��d���ǽ�ʯ���������������Һ�У�����������ҺΪ������Һ�����Կ���֪����Һ��ɫӦ������ɫ����D��������
��ѡD��
������ ������Ҫ����ʵ���������֪ʶ�����ʱӦ���ر�ע������֮�������ʱ����ɫ���Ƿ�����������ȷ����ʵ������
6.��2013•��������������¶���ڿ����У���������ٵ��ǣ�������
�� A�� Ũ���� B�� Ũ���� C�� �������� D�� �Ȼ���
���㣺 �����г�������ε����������ʱ仯�����淨��
ר�⣺ ���ʵı仯�����ʣ�
������ Ũ������н�ǿ�Ļӷ��ԣ�¶���ڿ������Ȼ���ӷ���Һ�������٣�Ũ�Ƚ��ͣ�Ũ���������ˮ�����������ӣ��Ȼ�����һ�ְ�ɫ����״���壬һ��¶���ڿ������������ᷢ���ı䣻�������Ʒ��ڿ������׳����Լ��Ͷ�����̼��Ӧ���������ӣ�
��� �⣺A��Ũ�����ӷ��������С����A��ȷ��
B��Ũ���������ˮ�ԣ����������ӣ���B����
C���������Ʒ��ڿ������׳����Լ��Ͷ�����̼��Ӧ���������ӣ���C����
D���Ȼ����ڿ����������������䣬��D����
��ѡA��
������ ���⿼�������ʵķ��ö���������Ӱ�죬��ɴ��⣬�����������е����ʵ����ʵ�֪ʶ���У�
7.��2013•���ݣ���������[Co��OH��2]�����ֽ⣬����������Һ��Ӧ������Ϳ�Ϻ�����ĸ�������Ʊ�����Ϊ����Co+2HCl=CoCl2+H2����CoCl2+2NaOH=Co��OH��2��+2NaCl����˵����ȷ���ǣ�������
�� A�� �������ͭ�Ļ�ѧ������ͬ B�� ��������������ˮ
�� C�� �������ܵĻ�ѧ�����ȶ� D�� �������ܿ����ڸ����Ȼ�������
���㣺 ��Ļ�ѧ���ʣ������Ļ�ѧ���ʣ�����ε��ܽ��ԣ�
ר�⣺ ��Ͽα�֪ʶ����Ϣ��
������ ��������ṩ�Ļ�ѧ����ʽ���з��������������ᷢ����Ӧ�������������ڼ�Dz�����ˮ�����ʣ��ݴ˽�ɣ�
��� �⣺A�����������ᷢ����ѧ��Ӧ����ͭ�������ᷴӦ��������ͭ�Ļ�ѧ���ʲ���ͬ����A����
B�����ݢڿ��Կ��������ɵ����������dz�������������ˮ�����ʣ���B��ȷ��
C���������������ֽ⣬�仯ѧ���ʲ��ȶ�����C����
D�������������ڼ�������ڸ����Ȼ������壬��D����
��ѡB��
������ ����Ϊ��Ϣ�����⣬��ɴ��⣬������������ṩ����Ϣ������ʵ����ʽ��У�
8.��2013•���������������ڿ�����¶��һ��ʱ�ʺ��������ᷢ���仯���ǣ�������
�� A�������� B�� �������� C�� Ũ���� D�� �Ȼ���
���㣺 �����г�������ε����������ʱ仯�����淨����ʯ�ҵ���������;��
ר�⣺ ���ʵı仯�����ʣ�
������ �������ʵ��������жϣ�����������ˮ�������������ڶ�����̼��Ӧ��Ũ���������ˮ�ԣ��Ȼ����ڿ����в��ᷢ���仯��
��� �⣺��������ı�������ڿ�����һ�㲻�ᷢ���仯����������������ˮ�֣������������ڿ����еĶ�����̼��Ӧ����̼��ƣ�Ũ��������ˮ�������ڿ����������������ӣ�ֻ���Ȼ����ڿ����в��ᷢ���仯����������ı䣮
��ѡD
������ �˽ⳣ�����ʵ������ǽ����������Ĺؼ����ڣ��ر���һЩ���ʵ���ˮ�Իӷ����Լ����ʵȵ����ԣ�
9.��2013•����������X�ɷ���������ʾ��������Ӧ����X�����ǣ�������
��X+�����+H2O ��X+�������������+H2O��
�� A�� Fe2O3 B�� CO C�� Ca��OH��2 D�� HCl
���㣺 ���ʵļ����ƶϣ�
ר�⣺ �������ʵ��ƶ��⣮
������ �������ʵ����ʣ����������ķ�Ӧ����������ᷴӦ�����κ�ˮ������������������ᷴӦ�����κ�ˮ��
��� �⣺��������ᷴӦ�����κ�ˮ������������������ᷴӦ�����κ�ˮ������X�����������ʣ�����ѡ����������ᣬ�������⣬��D��ȷ��
��ѡD��
������ ���⿼����������ʣ���ɴ��⣬��������������ʽ��У�
10.��2013•���ޣ������ǵ���Ҫ�ɷ���̼��ƣ���һ�����ʵļ�������ʢ������ϡ����IJ������У����Թ۲쵽����ð���ݣ������ݵ���Ҫ�ɷ��ǣ�������
�� A�� H2 B�� CO2 C�� O2 D�� N2
���㣺 ��Ļ�ѧ���ʣ�
ר�⣺ �������� ���ͨ�ԣ�
������ ̼����������ᷴӦ���ɶ�����̼���壬���Ծݴ˽����⣮
��� �⣺�����ǵ���Ҫ�ɷ���̼��ƣ�̼����������ᷴӦ���ɶ�����̼���壬���ɵĶ�����̼���帽�ڵ��DZ��棬����������ѡ�����֪��ѡ��B��ȷ��
��ѡB��
������ ����������֪ʶ������̼�������ķ�Ӧ����ɴ��⣬�����������е�֪ʶ���У�
11.��2013•���ޣ�һЩ�����ڳ����µĽ���pH���±���
|
���� |
Ѫ�� |
θҺ |
������ˮ |
����֭ |
|
PH |
7.35��7.45 |
0.9��1.5 |
��5.6 |
3.5��4.5 |
�����й������������ʵ�˵������ȷ���ǣ�������
�� A�� ֻ������֭������ B�� ֻ��Ѫ���Լ���
�� C�� ������ˮ������ D�� θ��������Ӧ����������֭
���㣺 ��Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ ��Ͽα�֪ʶ����Ϣ��
������ ������Һ���������pH֮��Ĺ�ϵ����������Һ��pH����7ʱ�������ԣ�����Һ��pH����7ʱ���ʼ��ԣ�����Һ��pHС��7ʱ�������ԣ�
��� �⣺A��θҺ��������ˮ������֭��pH��С��7���������ԣ���˵������
B��Ѫ����pH����7���Լ��ԣ�θҺ��������ˮ������֭��pH��С��7���������ԣ���˵����ȷ��
C��������ˮpH��5.6��С��7�������ԣ���˵������
D������֭pHΪ3.5��4.5��С��7�������ԣ����θ�������˲�Ӧ����������֭����˵������
��ѡB��
������ ���⿼���˻�ѧ�������֪ʶ����ɴ��⣬����������Һ���������pH�Ĺ�ϵ��֪ʶ���У�
12.��2013•���ޣ���ʢ��10mLNaOH��Һ�����е���������ɫ��̪��Һ�����ձ�����μ���ϡ���ᣬ��pH�ƣ�������ȷ�ⶨ��ҺpH���������ⶨ��Һ��pH�������������£�
|
����ϡ��������/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
�ձ�����Һ��pH |
12.9 |
12.7 |
12.5 |
12.3 |
11.9 |
7.0 |
2.1 |
1.9 |
��1��������ϡ��������Ϊ��10��mLʱ��NaOH��Һ��ϡ����ǡ����ȫ��Ӧ��
��2��������ϡ��������Ϊ3mLʱ����Һ�����졡ɫ��������ϡ��������Ϊ14mLʱ����Һ�����ޡ�ɫ��
��3�����ձ�����Һ��pH=2.1ʱ����Һ�е������У���NaCl��HCl����
���㣺 �кͷ�Ӧ����Ӧ�ã����ָʾ���������ʣ���Һ���������pHֵ�Ĺ�ϵ��
ר�⣺ �������� ���ͨ�ԣ�
������ ���������ܺ�ϡ���ᷢ���кͷ�Ӧ�����Ȼ��ƺ�ˮ������ϡ����IJ��ϼ��룬�������Ʋ��ϼ��٣�pH��С����pH����7ʱ��ǡ����ȫ��Ӧ��ϡ���ᳬ��10����ʱ����Һ�����ԣ���pH=2.1ʱ����Һ�����ԣ���ʱ��Һ�е����ʼ������ɵ��Ȼ��ƣ�����δ��Ӧ������ݴ˽��������з������
��� �⣺��1��pH=7ʱ���������ƺ�ϡ����ǡ����ȫ��Ӧ���ɱ������ݿ�֪����ʱ���ĵ�����������Һ�����Ϊ10ml��
��2����ɫ��̪��������Һ���ɫ�������Ժ�������Һ����ɫ��������ϡ��������Ϊ3mLʱ���ձ�����Һ��pH����7����Һ�Լ��ԣ���ʹ��ɫ��̪��Һ��죻������ϡ��������Ϊ14mLʱ���ձ�����Һ��pHС��7����Һ�����ԣ���ɫ��̪��Һ����ɫ��
��3����pH=2.1ʱ��ϡ�����������ʱ��Һ�е����ʼ������ɵ��Ȼ��ƣ�����δ��Ӧ�����ᣮ
�ʴ�Ϊ����1��10����2���죻�ޣ���3��NaCl��HCl��
������ �����ѶȲ��Ǻܴ���Ҫ�������кͷ�Ӧ����Ӧ�ã�������Һ������Ժ���ҺpH��С֮��Ĺ�ϵ����ͼ����ϵĽǶ������кͷ�Ӧ����ȷ�����Ĺؼ���
13��2013•���ݣ�ij��ѧ�о���ѧϰС����ѧϰ��Ļ�ѧ����ʱ�������ʵ�鷽������������ͼ��ʾ��ʵ�飬���������ϵ�֪��Na2CO3��Һ�ͳ����ʯ��ˮ���ʼ��ԣ�pH��7����CaCl2��Һ�����ԣ�pH=7����
��1����ʵ���У����з�̪������������Һ�����졡ɫ����μ���ϡ���ᣬֱ����Һǡ�ó���ɫΪֹ��
��2����ʵ���Թ��ڲ�����ɫ�������䷢����Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+Na2CO3=CaCO3��+2NaOH����
��3��ʵ�������ͬѧ�ǽ��ס�������ʵ��ķ�Һ����ͬһ���ձ��У��۲쵽��Һ�ʻ��Dz��Ժ�ɫ���ɴ˷�����֪��
����Һ�г�̼��ơ��Ȼ��ơ�ˮ��ָʾ���⣬һ�����������������ơ���
����������ʵ����̣�����Ϊ�����Һ�ʼ��Ե�������ɹ�����3���ֿ��ܣ�
��4���������ʵ���еij���ʯ��ˮ��ΪCaCl2��Һ��ͬ������ʵ�飨1����2����3���IJ�������Һ�ʻ��Dz��Ժ�ɫ�����������ܡ������������������������������֣�

���㣺 ��Ļ�ѧ���ʣ�̼���ơ�̼��������̼��ƣ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
ר�⣺ ѹ��ʵ���⣻�����ļ� ���ͨ�ԣ�
������ �������е�֪ʶ���з�������̪��Һ�ڼ�����Һ��Ϊ��ɫ��������������̼���Ʒ�Ӧ����̼��Ƴ������������ƣ�̼���ƺ��������Ʒ�Ӧʱ������ǡ����ȫ��Ӧ��Ҳ������������ʣ�ࣻ�Ȼ�������̼���Ʒ�Ӧ�����Ȼ��ƺ�̼��ƣ�ͬ���������ʹ�����������ݴ˽��
��� �⣺��1������������Һ�ʼ��ԣ���ʹ��̪��Һ��죬����죻
��2��̼���������������Ʒ�Ӧ����̼��Ƴ������������ƣ����Ca��OH��2+Na2CO3=CaCO3��+2NaOH��
��3���ٷ�̪��Һ�ڼ�����Һ��Ϊ��ɫ������̼�������������Ʒ�Ӧ�����������ƣ���һ�������������ƣ�����������ƣ�
����̼��������������ǡ����ȫ��Ӧ���������̼��ơ��Ȼ��ơ�ˮ��ָʾ���Լ��������ƣ���̼������ʣ�࣬�������̼��ơ��Ȼ��ơ�ˮ��ָʾ�����������ƺ�̼���ƣ���������������ʣ�࣬�������̼��ơ��Ȼ��ơ�ˮָʾ�����������ƺ��������ƣ���������������ϣ����3��
��4���ij��Ȼ�����Һ����̼������ʣ�࣬����̼������Һ�ʼ��ԣ�ͬ�����ܻ������Һ����ǵ���������ܣ�
������ ���⿼���˳������ʼ�ķ�Ӧ�Լ����ʷ�Ӧʱ���������̽������ɴ��⣬������������ṩ����Ϣ������ʵ����ʽ��У�
14��2013•�������������ϵ�֪������������Һ�� ����H2O��Na+��OH����ij��ѧ��ȤС��ͬѧ��̽������������Һ����һ��������ʹ��ɫ��̪��Һ��죬��������ʵ����ƣ�
ʵ��һ���ڵ�һ֧�Թ��м���Լ2ml����ˮ���ٵ��뼸����ɫ��̪��Һ���۲�ʵ������
ʵ������ڵڶ�֧�Թ��м���Լ2ml��5%NaCl��pH=7����Һ���ٵ��뼸����ɫ��̪��Һ���۲�ʵ������
ʵ�������ڵ���֧�Թ��м���Լ2ml��5%NaOH��Һ���ٵ��뼸����ɫ��̪��Һ���۲�ʵ������
��������ʵ��̽���ش��������⣺
��1��ʵ��һ�۲쵽������������Һ����ɫ�����ó��Ľ�������H2O����ʹ��̪��Һ��졡��
��2��ʵ����۲쵽������������Һ����ɫ�����ó��Ľ����ǣ�Na+����ʹ��ɫ��̪��Һ���ɫ��
��3��ʵ�����۲������������Һ��졡���ó��Ľ�������������������ʹ��̪��Һ��졡��
��4����չӦ�ã���μ�2��3����ɫ��̪��Һ������������Һ������ϡ������ǡ����ȫ��Ӧ����Һ����ɫ�仯������Һ�ɺ�ɫ��Ϊ��ɫ�����÷�Ӧ�Ļ�ѧ����ʽ����HCl+NaOH�TNaCl+H2O����
���㣺 ��Ļ�ѧ���ʣ�
ר�⣺ �����ļ� ���ͨ�ԣ�
������ ��1����Ϊ������ˮ�е��뼸����ɫ��̪��Һ����Һ��������ɫ������˵��H2O����ʹ��̪��Һ��죬���Ծݴ˽����⣻
��2�����Ȼ�����Һ�е��뼸�η�̪��Һ����ʱ��Һ��Ȼ����ɫ��˵��Na+����ʹ��̪��Һ��죬���Ծݴ˽����⣻
��3������̪��������������Һ�з�����Һ��죬�ۺ�����ʵ����Եó�������������ʹ��̪��죬���Ծݴ˽��
��4�����������������Һ��Ӧ���������Ե��Ȼ�����Һ�����Ե�����ǡ����ȫ��Ӧʱ��Һ��Ϊ��ɫ���÷�Ӧͬʱ������ˮ�����Ծݴ���ɽ��
��� �⣺��1����Ϊ������ˮ�е��뼸����ɫ��̪��Һ����Һ��������ɫ������˵��H2O����ʹ��̪��Һ��죻
��2�����Ȼ�����Һ�е��뼸�η�̪��Һ����ʱ��Һ��Ȼ����ɫ��˵��Na+����ʹ��̪��Һ��죻
��3������̪��������������Һ�з�����Һ��죬�ۺ�����ʵ����Եó�������������ʹ��̪��죻
��4�����������������Һ��Ӧ���������Ե��Ȼ�����Һ�����Ե�����ǡ����ȫ��Ӧʱ��Һ��Ϊ��ɫ���÷�Ӧͬʱ������ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��HCl+NaOH�TNaCl+H2O��
�ʴ�Ϊ����1����Һ����ɫ��H2O����ʹ��̪��Һ��죻
��2����Һ����ɫ��
��3����Һ��죻������������ʹ��̪��Һ��죻
��4����Һ�ɺ�ɫ��Ϊ��ɫ��HCl+NaOH�TNaCl+H2O��
������ ������Ҫ���黯ѧʵ�鷽������������ۣ�ѧ�����ò�������ʵ��֤�ķ����ͼ��ɴ���ʵ�����⣮
15��2013•���£�X��Y�ֱ�������������Һ��ϡ�����е�һ�֡���ͼ��X��
��Y��ʱ��ҺpH�ı仯����ͼ����ͼ�пɷ�����������Ϣ��
�磺X������������Һ��b�㴦����ҺpHΪ7�ȡ���
��д��������Ϣ������д3�㣩
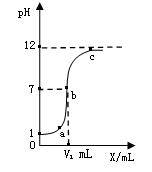

��1�� ��
��2�� ��
��3�� ��
16��2013•����������ʯ���к�һ������ϡ����ʱ����ʯ�������ᷴӦ�Ļ�ѧ����ʽΪ��Ca��OH��2+2HCl�TCaCl2+2H2O������ǡ����ȫ��Ӧʱ����Һ�е�����Ϊ���Ȼ��ơ���
���㣺 �кͷ�Ӧ����Ӧ�ã���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��3794729
ר�⣺ �������� ���ͨ�ԣ�
������ ���ݷ���ʽ����д������һд������ע���ĵȺţ���ǡ����ȫ��Ӧ������Ҫ�����������ң�
��� �⣺��Ӧ�����������ƺ����ᣬ���������Ȼ��ƺ�ˮ���ù۲취��ƽ���ɣ����Է���ʽ�ǣ�Ca��OH��2+2HCl�TCaCl2+2H2O����ǡ����ȫ��Ӧʱ����Ӧ���Ѿ�û���ˣ�������Һ�е�����Ҫ�����������ң����Ȼ��ƣ�
�ʴ�Ϊ��Ca��OH��2+2HCl�TCaCl2+2H2O���Ȼ��ƣ�
������ �����ؼ���Ҫ��Ϥ����ʽ����д������֪����Һ�����ʵ��жϷ���������������ٿ��Ƿ�Ӧ���Ƿ�������⣮

ͨѶ��ַ: ��������������Իƴ�����Է ��510660�����䣺lzm6308@163.com ��ϵQQ:534386438
Copyright © 2008-2012 klxkc.com All Rights Reserved. ��ICP��15026984��-1
